Прогнозування стабільності ферментів
Команда QuData провела дослідження з прогнозування термостабільності ферментів — ключових біологічних каталізаторів, що відіграють важливу роль у медицині, харчовій промисловості та сільському господарстві. Для вирішення цього завдання було розроблено ансамблевий підхід, що поєднує нейромережі (3D-ResNet), структурні дескриптори MoleculeKit та оцінки Rosetta. Така комбінація дозволяє точно передбачати стабільність білків за їх амінокислотними послідовностями та структурними ознаками, що допомагає краще розуміти поведінку ферментів і підвищує ефективність їх використання в промисловості та білковій інженерії.

 Завдання
Завдання
Ферменти (ензими) – це білки, які діють як каталізатори у хімічних реакціях в живих організмах. Вони відіграють фундаментальну роль у різних біологічних процесах і застосовуються в багатьох галузях промисловості. Ферменти додають при виробництві харчових продуктів і напоїв, покращуючи якість продукції. Вони використовуються у розробці фармацевтичних препаратів і життєво важливі для перетворення біомаси на біопаливо. Це лише кілька прикладів різноманітного застосування ферментів.
Однак важливо зазначити, що багато ферментів мають проблеми, пов’язані зі стабільністю, особливо в суворих умовах. Ця нестабільність не тільки впливає на їх продуктивність, але й обмежує кількість білка, який може вироблятись у клітині. Тому існує нагальна потреба в ефективних обчислювальних методах для прогнозування та підвищення стабільності білка, що викликає значний інтерес як у технічній, так і в науковій сферах.
Розуміння та точне прогнозування стабільності білків є фундаментальною проблемою в біотехнології. Ці знання мають широке застосування: від підвищення продуктивності дії ферментів до вирішення глобальних проблем у сфері сталого розвитку чи вуглецевої нейтральності. Підвищення стабільності ферментів може прискорити швидкість перебігу наукових експериментів та зменшити витрати на їх проведення.
 Огляд рішення
Огляд рішення
Метою нашого дослідження було спрогнозувати термостабільність різних ферментів. Експериментально виміряні дані про термостабільність (температура плавлення) охоплювали як природні послідовності, так і послідовності, які були створені за допомогою поодиноких або декількох мутацій на основі природних послідовностей.
Успішне рішення цього завдання сприяє вирішенню основної проблеми щодо покращення стабільності білків, що дозволить швидше та вигідніше створювати нові білки, у томі числі високовартісні ферменти та лікарські препарати.
Під час дослідження наша команда перш за все використала певний підхід під назвою "Thermonet", який продемонстрував обнадійливі результати.
Ми експериментували з різними архітектурами нейронних мереж і обрали спрощений варіант, який показав хороші результати. Для подальшого вдосконалення наших прогнозів ми використали такий інструмент як "molekulekit" для створення дескрипторів ознак і ще більше покращили продуктивність моделі.
Крім того, команда QuData виявила, щоЗагалом, проведене дослідження підкреслює важливість оцінок Rosetta і середнього значення параметра донора водневих зв’язків для прогнозування термічної стабільності ферментів.
Наше дослідження було ініційоване конкурсом, який провела організація Novozymes. Учасникам запропонували створити модель для прогнозування та ранжування термостабільності різних ферментів на основі експериментальних даних про температуру плавлення, отриманих від дослідницької лабораторії Novozymes. Ознайомитись з подробицями змагання та результатами дослідження можна тут.


 Технічні деталі
Технічні деталі
Прагнучи покращити прогнози термічної стабільності команда QuData дослідила різні стратегії та технології. Нижче наведено ключові етапи розробки нашого підходу.
Початкова стадія – nesp-thermonet: ми почали з того, що визнали здатність підходу "nesp-thermonet" добре прогнозувати термостабільність ферментів.
Дослідження архітектур нейронних мереж: далі ми детально вивчили інформацію, наведену в цій статті, що спонукало нас дослідити різні архітектури нейронних мереж. Зрештою, ми обрали модель Resnet-3D.
Обрізка та спрощення нейронної мережі: для подальшого аналізу архітектури та визначення ключових факторів, які впливають на прогнозування, ми застосували ітеративний процес обрізки, що призвело до розробки спрощеної архітектури. Ця архітектура має такі самі вхідні дані, що і при використанні "Thermonet", (14,16,16,16,16).
Використання дескрипторів ознак: щоб покращити наші прогнозні показники, ми використали дескриптори ознак, створені за допомогою утиліти "molekulekit". За допомогою експериментів ми визначили оптимальні дескриптори з розміром блоку 16 і розміром вокселя 0,5. Така оптимізація підвищила прогнозні показники і сприяла створенню моделі "AVGP3", яка згодом була інтегрована в фінальний ансамбль.
Дослідження показників Rosetta: на основі відомостей, представлених в Deletion-specific ensemble, ми спостерігали за можливостями оцінок Rosetta прогнозувати термостабільність. Ми інтегрували оцінки Rosetta з моделлю "AVGP3" в ансамбль. Потім ми об’єднали модель "AVGP3" із ансамблем Deletion-specific, використовуючи певні вагові розподіли (0,2 і 0,8).
Використання таблиці "Pose_Energies": ми ретельно вивчили внесок оцінок Rosetta, проаналізувавши таблицю "Pose_Energies" у файлах pdb, що містить 20 параметрів і пов'язані з ними вагові коефіцієнти. Ці параметри відіграли ключову роль у створенні нашого підходу.
Рейтинг ансамблю Rosetta: під час наших досліджень сформувався інноваційний підхід, який передбачав використання вагових коефіцієнтів для ансамблю. Незалежні прогнози термостабільності були згенеровані для кожного параметра окремо для всіх мутацій. Потім ці індивідуальні прогнози були об’єднані в конфігурацію ансамблю з використанням вагових коефіцієнтів із таблиці "Pose_Energies". Цей ансамбль було названо "RankedRosetta".
Фінальна інтеграція ансамблю: остаточний результат з форумів спільноти був інтегрований в наш ансамбль, що ще більше підвищило загальний показник. Формула інтеграції була виражена як (0,05 * Rasp + 0,95 * 0,615).
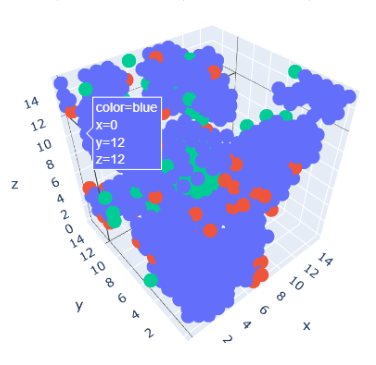
Як підсумок, ми можемо стверджувати, що комплексний підхід нашої команди QuData привів до помітних результатів. Наше дослідження визначило вагомий вплив оцінок Rosetta на всю молекулярну структуру, а також вплив середнього параметра донора водневих зв’язків поблизу місць мутацій на прогноз термостабільності ферментів.
